Sindrom propusnog crijeva (Leaky Gut Syndrome)
Po svojoj površini probavni trakt predstavlja najveće sučelje između organizma i vanjskog svijeta. Kod odraslih se otprilike 1 tona hranjivih tvari godišnje transportira kroz “granični zid probavnog trakta”. Istodobno, crijevna sluznica predstavlja vrlo učinkovitu barijeru koja priječi apsorpciju nedovoljno razgrađenih komponenti hrane, bakterijskih endotoksina, anorganskih toksina i teških metala. Različite nokse mogu dovesti do oštećenja ove barijere, čime se povećava rizik nekontroliranog ulaska antigena u laminu propriu, ali i u sistemsku cirkulaciju. Nekontrolirani dotok antigena potiče lokalne i sustavne imunološke reakcije, koje često mogu biti odgovorne i za razvoj ozbiljnih bolesti.
Nakon što prođu kroz mukozni sloj na površini sluznice crijeva, molekule i antigenske strukture iz crijeva kroz neoštećenu crijevnu barijeru uglavnom ulaze putem slijedeća tri puta:
- kroz M stanice (preuzimanje antigena),
- kroz enterocite (stanična propusnost)
- kroz tijesne međustanične spojeve (parastanična propusnost). Potonji ujedno štite crijevnu sluznicu od prolaska egzogenih supstrata iz lumena crijeva u međustanični prostor.
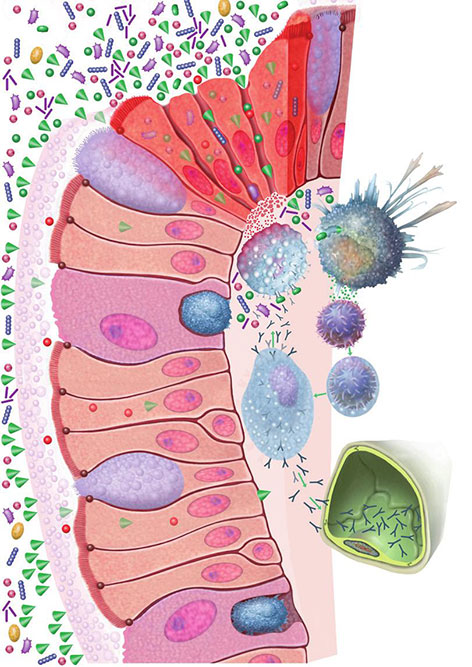
Tijesni međustanični spojevi, tzv. zonula occludens, područja su koja međusobno čvrsto povezuju pojedinačne enterocite u kompaktnu staničnu strukturu koja postaje funkcionalna barijera s vrlo aktivnom i učinkovitom transportnom ulogom.
Ti čvrsti međustanični spojevi su građeni od različitih transmembranskih proteina (okludin, JAM, različiti klaudini) i do sada su identificirana 24 različita klaudina, koji imaju i različite funkcije. Moglo bi se reći kako ionska propusnost ovih spojeva ovisi o specifičnom sastavu klaudina. S druge strane, JAM protein (junctional adhesion molecule) ima uglavnom građevnu ulogu u osiguranju kohezije anatomske strukture čvrstih spojeva.
Brojni čimbenici, posebice različite bolesti, stres, lijekovi, alkohol, nikotin, mikroorganizmi, bakterijski toksini, proupalni citokini itd, mogu značajno narušiti integritet epitelnih stanica i tijesnih međustaničnih spojeva čime epitel postaje propusan za alergene, toksine i patogene. Nekontrolirani prolaz tih štetnih čimbenika iz lumena crijeva dodatno oštećuje crijevnu barijeru što na kraju dovodi do značajnog poremećaja njene funkcije, odnosno do razvoja sindroma propusnog crijeva (Leaky Gut Syndrome).
Gubitak funkcije crijevne barijere, npr. kod upalne iritacije sluznice (vidi segment enterocita prikazanih crvenom bojom na slici 1), između ostalog značajno povećava rizik od senzibilizacije. Povećana propusnost sluznice rezultira nekontroliranim priljevom antigena u laminu propriju. Pokreću se imunološke kaskade koje preko razvoja preosjetljivosti (npr. na komponente hrane) i povećanog stvaranja antitijela dovode do pojačanog oslobađanja medijatora upale koji onda dodatno oštećuju strukture epitelnih stanica i čini ih još propusnijim te na kraju nastaje začarani krug.
Zonulin u serumu ili u stolici, alfa-1-antitripsin u stolici i lipopolisaharidi (LPS) u serumu ključni su laboratorijski pokazatelji u procjeni funkcije i stupnja propusnosti crijevne sluznice. Osim njih, vrlo važnu ulogu u postavljanju ispravne dijagnoze imaju i dodatni parametri iz stolice, kao što su kalprotektin, lizozim, EPX i slgA čijim određivanjem se precizno procjenjuje crijevna upalna aktivnost.
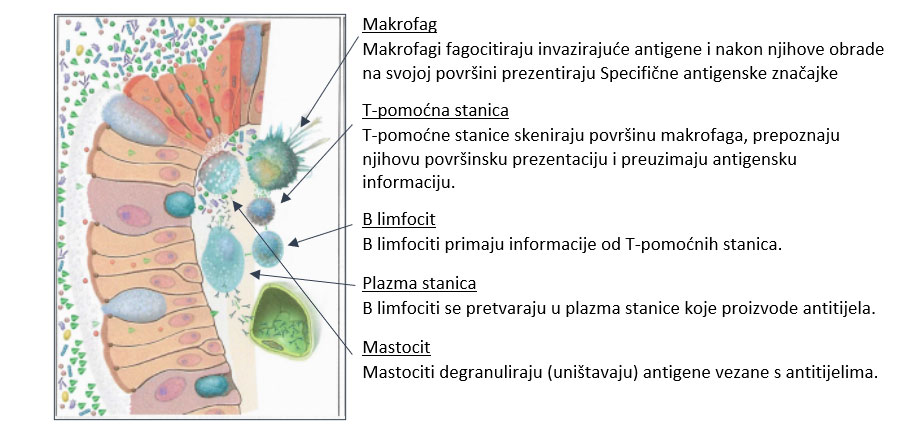
Slika 1: Sindrom propusnog crijeva – Gubitak funkcije crijevne barijere
Posljedice povećane propusnosti crijeva
Kao što je već rečeno različite bolesti mogu negativno utjecati na crijevnu propusnost i tako uzrokovati razvoj sindroma propusnog crijeva, ili tzv. sindroma curenja crijeva (Leaky Gut Syndrome). Posljedično, ovo stanje može dovesti do razvoja ozbiljnih poremećaja kao što su:
- Crijevna upala
- Neadekvatna apsorpcija hranjivih tvari iz crijeva
- Stvaranje antitijela zbog prolaza antigena visoke molekularne težine
- Stvaranje cirkulirajućih imunoloških kompleksa
- Pokretanje autoimunih reakcija unakrsnim reakcijama na vlastite strukture tijela
- Stvaranje autoreaktivnih T stanica
Ulazak bakterija i bakterijskih produkata u krvotok potiče pojačanu imunološku aktivaciju i pojavu sustavnih upalnih reakcija. Glavne kliničke posljedice su kronične infekcije, kardiovaskularni poremećaji, alergije i autoimune bolesti.
Intolerancija na hranu, koja se može utvrditi IgG testovima, također se smatra posljedicom poremećene crijevne propusnosti. Čini se da vrsta i količina preuzetih antigena iz crijeva ipak igra vrlo značajnu ulogu u imunološkoj diferencijaciji imunološkog sustava sluznice. Nefiziološki priljev visokog titra antigena u kontakt s imunološkim strukturama crijeva inhibira regulatorne mehanizme sluznice i dovodi do indukcije stvaranja antitijela i nastanka imunoloških kompleksa. Sukladno tome sve je više pokazatelja koji pokazuju kako pojava IgG protutijela protiv pojedinih sastojaka hrane ipak nije uobičajeni fiziološki proces, kao što to sugerira trenutno prevladavajuće mišljenje.
Također je dokazano postojanje veze između povećane crijevne propusnosti i nastanka nitrostresa. Naime, povećana propusnost endotoksina gram-negativnih bakterija dovodi do nitrostresa putem stimulacije NF-kappaB, COX-2 i inducibilne NO-sintetaze.
Na kraju valja istaknuti kako povećanu propusnost tijesnih međustaničnih spojeva mogu uzrokovati i neki fiziološki spojevi kada su prisutni u suvišku, posebice biogeni amini, kao npr. histaminoza kod osoba s intolerancijom na histamin, adrenalin kod vrlo snažnog stresa i sl.
Laboratorijska dijagnostika
- ZONULIN
Zonulin je jedini mjerljivi protein u krvi koji odražava crijevnu propusnost, a povećane razine zonulina smatraju se ključnim markerom narušene crijevne barijere. Zonulin je humani analog vrlo sličan toksinu Vibrio cholerae koji otpušta tijesne spojeve tankog crijeva i na taj način značajno povećava propusnost tankog crijeva. Zonulin se izlučuje uglavnom iz jetre i enterocita, međutim u određenoj mjeri ga luče i stanice masnog tkiva, mozga, srca, imunološkog sustava, pluća, bubrega i kože.
Pojačano, nefiziološko izlučivanje zonulina mogu potaknuti bakterije, ali i različiti toksini iz hrane kao npr. gluten. Tako je utvrđeno kako bolesnici s aktivnom celijakijom imaju značajno višu razinu zonulina u usporedbi s osobame bez nje, kao i u usporedbi s bolesnicima u remisiji, odnosno na dijeti bez glutena.
Sve je više dokaza koji ukazuju na postojanje uske povezanosti između povećane propusnosti crijeva i različitih autoimunih bolesti. Brojna ispitivanja na životinjskim modelima su pokazala kako povećanje razine zonulina i povećana propusnost crijevne stijenke prethode nastanku dijabetesu tipa 1. Štoviše, u nekim studijama na životinjskim modelima blokiranjem zonulina se preveniralo razvoj dijabetesa tipa 1. Također je zabilježeno kako mnogi pacijenti s celijakijom često pate i od drugih autoimunih bolesti. Stoga se smatra kako povišene razine zonulina igraju važnu ulogu u patogenezi celijakije, ali i drugih autoimunih bolesti kao što su dijabetes ovisan o inzulinu, multipla skleroza, reumatoidni artritis i sl.
Zonulin je vrlo osjetljiva i specifična metoda za procjenu funkcije barijere crijevne sluznice, čije određivanje ima važnu ulogu u rutinskoj dijagnostici posebice celijakije, ali i ostalih autoimunih bolesti poput Inzulin ovisnog dijabetes melitusa, Multiple skleroze, Reumatoidnog artritisa i dr.
Zonulin se može određivati u serumu i u stolici.
- ENDOTOKS(IN)EMIJA
Povećana koncentracija sastavnica stanične stijenke gram-negativnih bakterija, tzv. lipopolisaharida (LPS) u serumu naziva se endotoksinemija i također je važan, direktni pokazatelj poremećene propusnosti crijeva (slika 2).
U nekim dijelovima probavnog trakta je prirodno prisutna stalna flora mikroorganizama koja tvori stabilan ekosustav. Unatoč visokoj kolonizaciji bakterija u lumenu debelog crijeva, organizam u fiziološkim uvjetima osigurava njihovu izoliranost i održava sterilnost susjednih funkcionalnih odjeljaka i organa priječeći translokaciju potencijalno patogenih klica.
Sluz, intaktni epitel i lamina propria crijevne stijenke čine učinkovitu barijeru prolazu bakterija i njihovih komponenti, tako da samo vrlo male količine endotoksina iz Gram-negativnih bakterija mogu eventualno doprijeti u krv. Promjena ravnoteže crijevne flore u korist gram-negativnih bakterija ili poremećaj barijerne funkcije crijevne sluznice, dovest će do povećanja translokacije ovih endotoksina u cirkulaciju.
Bakterijski endotoksini, također poznati kao lipopolisaharidi (LPS) su toplinski stabilne komponente vanjske stanične stijenke gram-negativnih bakterija koje se oslobađaju nakon što bakterijske stanice odumru. Endotoksini su građeni od molekularne jezgre, koju čini prilično uniforman lipofilni lipida A i različitih hidrofilnih polisaharidnih bočnih lanaca specifičnih za vrstu. LPS su izuzetno snažan aktivator stanica imunološkog sustava. Različiti pro-upalni medijatori, oslobođeni iz tako LPS-aktiviranih stanica imunološkog sustava uzrokuju nastanak sistemskog upalnog odgovora koji u najtežem obliku za posljedicu može imati razvoj endotoksičnog šoka s teškim metaboličkim i kardiovaskularnim oštećenjima.
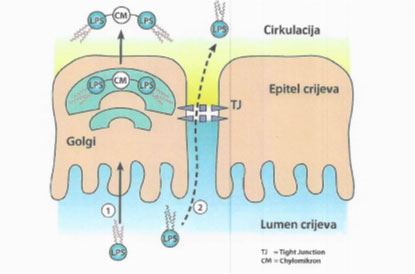
Slika 2: Translokacija LPS-a iz crijeva (modificirano od Caesar et al., 2010.)
- ALFA-1 ANTITRIPSIN
Alfa-1-antitripsin je protein koji inhibira različite proteolitičke enzime tzv. proteaze. Primarno nastaje u jetri, ali se manjim dijelom stvara i u sluznici crijeva. Kod oštećene funkcije crijevne barijere, npr. kod upalnih stanja u crijevu, pojačana propusnost crijevne sluznice je dvosmjerna pa tako između ostalog dolazi i do pojačanog gubitka proteina u lumen crijeva (proteinska enteropatija).
Budući da je uglavnom vrlo otporan na proteolitičko djelovanje kako endogenih, crijevnih proteaza tako i egzogenih proteaza bakterija i drugih mikroorganizama crijeva, alfa-1-antitripsin praktički nepromjenjen dospijeva u feces, zbog čega se pokazao kao najoptimalniji marker za određivanje stupnja oštećenja crijevne barijere i gubitka proteina u lumen crijeva. Njegovo određivanje u stolici vjerodostojno odražava stupanj propusnosti crijevne barijere.
Međutim, važno je napomenuti kako negativan nalaz alfa-1 antitripsina ne isključuje postojanje pojačane propusnosti crijeva, jer kod blažeg oštećenja crijevne barijere molekule alfa-1 antitripsina mogu biti prevelike za trenutni stupanj oštećenja. Stoga je vrlo važno nalaz alfa-1 antitripsina u stolici interpretirati u kontekstu ostalih parametara oštećenja crijevne barijere. Osim toga, za ispravnu interpretaciju oštećenja crijevne barijere važno je uz alfa-1 antitripsin u stolici odrediti i vrijednost alfa-1 antitripsina u serumu.
